Polytetrafluoroethylene (polytetrafluoroethylene) probabiliter maxime fluoropolymer usus est quia varias notas habet quae materiam idealem pro amplis applicationibus amplis efficiunt.Est flexibilior quam ceterae tibiae similes et omnes fere oeconomiae industriales resistere possunt
Cursus temperatus est circiter -330°F ad 500°F, quod latissimum intervallum inter fluoropolymeros temperaturas praebens.Praeterea habet egregias proprietates electricas et magneticam permeabilitatem humilem.Ptfe Tubing est maxime usus laboratorium Tubingae et applicationes ubi chemicae resistentia et puritas essentiales sunt.PTFEvalde humilis attritionis coefficiens est et una e substantiis "lapsi" notis
Features:
C% pura PTFE resinae
Comparati cum FEP, PFA, HP, PFA, UHP, PFA, ETFE, ECTFE, tibiae fluoropolymer flexibiles.
Chemice pigra, fere omnibus oeconomiae industrialibus et menstrua repugnantis
Lata temperatus range
Humilis penetratio
Smooth metam superficies non-baculus
Lowest friction coefficientes
Optimum electrica perficientur
Non flammabiles
Non toxic
Applicationes:
laboratorium
Processus chemica
Analysis et processus armorum
Emissio magna
Humilis temperatus
caliditas
Electricity
ozone
PTFE moleculis structura
Polytetrafluoroethylene (PTFE) facta est a polymerizatione tetrafluoroethylene multorum moleculorum.
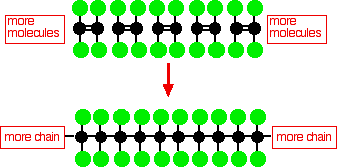
Hoc schemate simplex PTFE tres dimensiones moleculi structuram non ostendit.In simpliciori poly(ethylene) os carbonis moleculi connexum est solum ab atomis hydrogeniis, quae catena admodum flexibilis est, certe non est moleculae linearis.
Nihilominus, in polytetrafluoroethylene, atomus fluorinus in coetus CF2 satis magna est ut atomum fluorinum in coetus adjacentium impediat.Meministis omnem fluorinum atomum 3 paria electrons sola exserta
Effectus huius est ut rotationem carbonis carbonis unius vinculi supprimat.Atomi fluorini tendunt ad se ita dispositi, ut ab atomis fluorinis adjacentibus quam longissime absint.Rotatio tendit ad collisiones solas inter atomos fluorinos in atomis carbonibus adjacentibus, quae rotationem enixe adversam facit.
Vis repulsiva moleculae in figuram virgae claudit, et atomi fluorini in spiram valde leni dispositae; atomi fluorini in spiram circa os carbonis componuntur.Hae bracteae plumbeae in cistella instar penicilli longi et tenues comprimentur
Haec arcta dispositio notorum magnam vim habet in viribus intermolecularibus, ut videbis
Vires intermoleculares et punctum liquescens PTFE
Punctum liquationis polytetraflu-orethylene adfertur 327°C.Hoc polymerum hoc satis altum est, ut magnae sint oportet van der Waals vires inter moleculas
Cur homines van der Waals copias in PTFE debiles vindicant?
Van der Waals vis dispersionis causatur per dipoles fluctuantes temporales generatos cum electrons in moleculo circumagitur.Quia molecula PTFE magna est, crederes vis magnam dissipationem quia multum electronica sunt quae movere possunt.
Communis locus est, quo maior moleculae, eo maior dissipatio potestatis est
Sed PTFE quaestionem habet.Fluorinum valde electronegativum est.Electrona in vinculo carbo-fluorino arcte inter se ligare tendit, ita arcte ut electronica movere non possit ut cogitas.Carbo-fluorinum vinculum describemus quasi validum polarizationem non habentem
Copiae Van der Waals etiam interactiones bipoli-dipole includunt.Sed in polytetrafluoroethylene (PTFE), quodlibet moleculae circumdatur iacuit atomorum fluorinorum leviter negate.In hoc casu, sola possibilis commercium inter molecularum est mutua repulsio!
Ita vis dissipatio imbecillior est quam putas, et commercium bipole-dipole repulsio causabit.Minime mirum dicunt homines van der Waals vim in PTFE valde infirmam esse.Vim repulsivam actu non obtinebis, quia maior vis dispersionis quam commercii dipole-dipoli, sed rete effectus est quod vis van der Waals debilitare tendet.
Sed PTFE punctum altissimum liquefaciens, oportet quod vis, quae simul moleculas tenet, validissima sit
Quomodo PTFE altum punctum liquescens habere potest?
PTFE valde crystallina, hoc sensu area magna, moleculae sunt admodum regulares.Memento, PTFE moleculis ut baculi elongati cogitari possunt.Hi cardines arcte conglobatae erunt
Hoc significat, licet moles ptfe non possit revera magnas dipoles temporales producere, dipoles valde efficaciter adhiberi possunt.
Itane exercitus van der Waals in PTFE debilis vel fortis est?
Iudico utroque recteque te sit!Si vincula polytetrafluoroethylene (PTFE) ita disposita sunt ut inter catenas non nimis arcta contactu sit, vis inter eas valde debilis erit et punctum liquescens nimis erit infimum.
At moleculae in rerum contactu sunt.Van der Waals copiae non tam potentes esse possunt quam sint, sed structuram PTFE significat quam vim maximam sentiunt, altiore vincula intermoleculares validas producentes et puncta alta liquefacientia.
Hoc est contra alias copias, ut vi commercium bipoli-dipole, quae tantum per 23 vicibus reducitur, vel bis spatium reducitur per octo tempora.
Ergo stricta sarcina massae virgae informis in PTFE efficaciam dispersionis maximizat
Non-baculus possessiones
Quam ob rem aqua et oleum superficiei PTFE non haerent, et quare ova frigere potes in TPFE cacabo sine sartagine adhaerente.
Considerare debes quantas vires alias moleculas in superficie figere possentPTFE.Potest includere aliquod genus vinculi chemici, vi vel vinculi hydrogenii van der Waals
Vinculum chemicum
Vinculum carbon-fluorinum valde validum est, et impossibile est ut aliqua alia moleculae carbonis catenae attingant ad causam omnem substitutionis reactionem fiendam.Fieri non potest ut nexum chemical
van der Waals copiae
Vidimus vim van der Waals in PTFE non valde firmam esse, et tantum PTFE altum punctum liquescens habere, quia moleculae tam propinquae sunt ut contactum efficacissimum habeant.
Differt autem ab aliis moleculis prope superficiem PTFE.Moleculae relative parvae (ut moleculae aquae vel moleculae olei) tantum parvam contactum cum superficie habebunt et tantum parva attractio van der Waals generabitur.
Moleculum magnum (qualis interdum) non erit virga-formatum, ideo non satis efficax contactus inter illam et superficiem ad humiliationem polarizationem tendentiam PTFE superandam.
Utroque modo vis van der Waals inter superficiem PTFE & res circumiacentes parva est et inefficax
Consectetuer vincula
Molculae PTFE in superficie penitus ab atomis fluorinis involutae sunt.Hi atomi fluorini valde electronegativi sunt, ergo omnes aliquem gradum negationis accusant.Quisque Fluorine etiam habet 3-jugis oblongum sola electrons
Hae sunt condiciones ad vincula hydrogenii formationis requisita, ut solitarius par in fluorino et in aqua hydrogenii atomi.Sed hoc manifesto non fiet, alioquin erit vehemens attractio inter moleculas PTFE et moleculas aquarum, et aqua adhaerebit PTFE.
Summarium
Nulla via efficax est aliis moleculis ad superficiem PTFE feliciter applicandam, ideo superficies non baculo habet.
Humilis friction
Attritionis coefficiens PTFE valde humilis est.Id est, si superficiem linitam ptfe habeas, alia facile labuntur.
Infra promptum est compendium rei.Hoc venit ex charta 1992 inscripta "Frictio et Gere de Polytetrafluoroethylene".
Principio lapsus, superficies PTFE erumpit et massa transfertur in ubicunque illabatur.Hoc significat superficiem PTFE utetur.
Ut illapsum continuatur, caudices in tenues membranas explicantur.
Eodem tempore, superficies PTFE evulsa est ad constituto stratum formandum.
Utraeque superficies in contactu nunc habent moleculas bene ordinatas PTFE quae in alterutrum labi possunt
Haec introductio polytetrafluoroethylene, polytetrafluoroethylene in varios productos fieri potest, peculiariter nos facit in fistulam ptfe.ptfe caligarum manufacturersgratissimum nobis communicandum
Investigationes ad caligarum ptfe pertinentes:
Post tempus: May-05-2021





